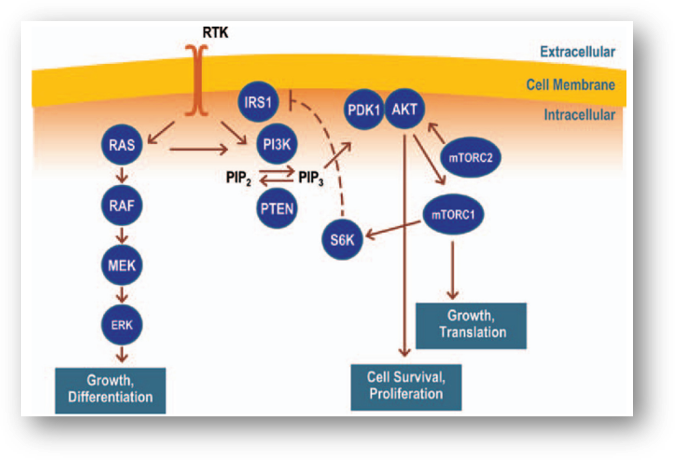
PI3K-Akt-mTOR信号通路的异常主要包括PIK3CA基因的突变和扩增、PTEN的缺失或突变、AKT1/2/3基因的突变或过表达、TSC1/2的突变。超过80% PIK3CA基因突变发生在螺旋区和激酶区[3]。PIK3CA基因的突变和扩增在乳腺癌、结直肠癌、胃癌、宫颈癌、前列腺癌和肺癌中都有报道。
目前针对PIK3CA基因突变已经开发了多个小分子抑制剂,根据作用靶点可以分为以下几类。其中大多数分子都因为疗效未达预期或毒副作用而失败,还有一些仍处于早期临床试验阶段。接下来,我们将简单介绍一下PIK3CA基因在以下四种常见实体瘤中的突变特征、临床意义和关键临床试验。
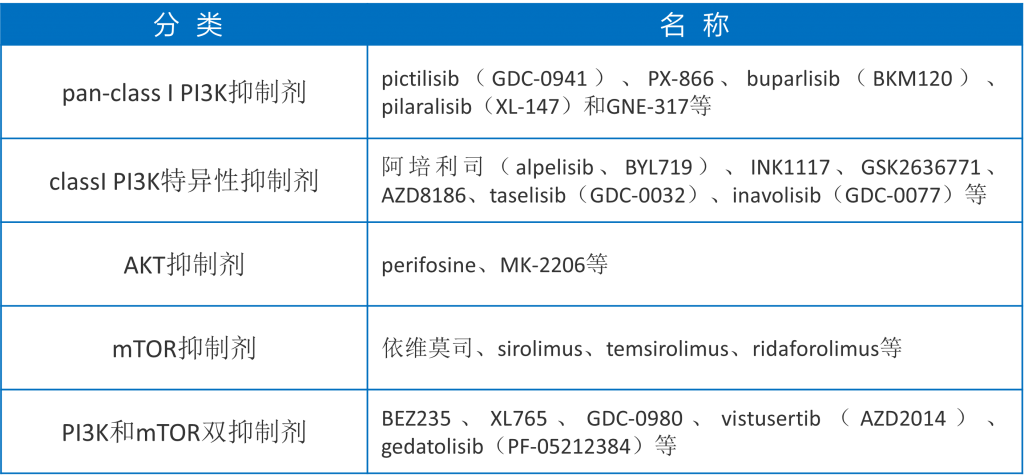
PI3K-Akt-mTOR信号通路是乳腺癌中最常发生突变的通路之一,文献报道的该通路基因在乳腺癌中的突变频率分别为:PIK3CA(36%)、PIK3R1(3%)、PTEN(3%)、AKT1(2%)[4]。在乳腺癌中,PIK3CA基因以9号外显子上的E542K和E545K突变,20号外显子上的H1047R突变最常见。阿培利司(alpelisib)是一种有效的选择性p110α抑制剂;FDA已批准阿培利司联合氟维司群治疗携带PIK3CA突变的激素受体阳性(HR+)/人表皮生长因子受体2阴性(HER2-)的局部晚期或转移性乳腺癌患者。目前在PIK3CA突变的局部晚期或转移性乳腺癌患者中开展早期临床试验的还有选择性p110α抑制剂inavolisib(NCT03006172)等。在去年的圣安东尼奥乳腺癌研讨会(SABCS 2021)上,知名药企Genetech公布了inavolisib联合氟维司群在PIK3CA突变,HR+/HER2-乳腺癌中的早期结果。在疗效可评估的49例患者中,12例患者达到部分缓解,初步的中位PFS为7.1个月[5]。
PIK3CA基因是结直肠癌中最常突变的基因之一,突变频率约为10-20%。尽管目前PIK3CA突变是否与结直肠癌患者的预后相关的结论并不一致,但最新的一项meta分析结果显示PIK3CA突变与EGFR的疗效无关[6]。在今年的ASCO上公布了一项mTOR抑制剂坦罗莫司(temsirolimus)的篮子研究的结果。TAPUR研究共纳入了10例接受temsirolimus单药治疗的,携带PIK3CA基因突变的CRC患者。从疗效来看,未观察到缓解的患者,有一例患者的疾病稳定,疾病控制率10%,提示temsirolimus单药对于PIK3CA突变的CRC患者并没有足够的临床活性[7]。
PIK3CA基因是宫颈癌中最常突变的基因之一,其中PIK3CA E545K突变在宫颈癌中的频率约为23-36%[8]。目前,PIK3CA突变是否与宫颈癌患者的预后相关的结论并不一致,但一项meta分析结果显示携带PIK3CA突变的宫颈癌患者的预后较差[9]。
与肺腺癌相比,PIK3CA基因突变在肺鳞癌中更常见(低于10%);同时,PIK3CA基因的扩增在肺鳞癌中也更常见,可高达30%。此外,PIK3CA基因突变常与EGFR、KRAS突变同时存在[10]。有研究报道PIK3CA基因突变与EGFR TKIs的获得性耐药性之间并没有明确的相关性[11]。
目前,其它正在PIK3CA突变的实体瘤中开展临床试验的有pan-PI3K抑制剂copanlisib、PI3Kα抑制剂CYH33、PI3K/mTOR双抑制剂gedatolisib等。其中,copanlisib已经被FDA批准用于至少接受过两次系统治疗的成人复发滤泡型淋巴瘤患者。CYH33在一项Ia期研究(NCT03544905)中表现出理想的抗肿瘤活性;NCT03544905是一项first-in-human临床研究;在42例疗效可评估患者中,28例患者携带PIK3CA突变;其中4例达到部分缓解,包括2例为卵巢癌患者和2例乳腺癌患者,客观缓解率为14.3%(4/28)、疾病控制率为46.4%(13/28)[12]。
针对以上基因,作为新一代液态活检精准医疗国际领军企业——慧渡医疗,自主研发的针对外周血的液态活检产品和MRD检测产品,具有灵敏度高和样本量要求量低的优势。慧渡医疗系列基因检测产品获得欧盟CE认证和英国UKCA认证(点击查看原文), 最近获得美国FDA突破性医疗器械(BDD)认定(点击查看原文),这是国际权威监管机构对慧渡医疗技术、产品和其临床应用价值的认可。
慧渡医疗新一代液态活检系列产品正在应用于位居世界500强的全球排名前十的国际顶尖药企和美国哈佛大学等国际顶级学术机构开展的众多临床研究,为ctDNA液态活检应用于药物临床试验并且服务全球肿瘤患者打下了坚实的基础。
参考文献:
[1] Hay N, Sonenberg N. Upstream and downstream of mTOR. Genes Dev. 2004 Aug 15;18(16):1926-45. [2] Chalhoub N, Baker SJ: PTEN and the PI3-kinase pathway in cancer. Annu Rev Pathol 4:127-150, 2009. [3] High frequency of mutations of the PIK3CA gene in human cancers. Science. (2004) 304:554. [4] Cancer Genome Atlas Network. Comprehensive molecular portraits of human breast tumours. Nature. 2012 Oct 4;490(7418):61-70. [5] Cancer Res (2022) 82 (4_Supplement): P5-17-05. [6] Cancer Res,2022;82(12_Suppl),Abstract#nr 1239. [7] JCO.2022.40.4_suppl.106, Abstract#106. [8] Zhang L, Wu J, Ling MT, et al. The role of the PI3K/Akt/mTOR signalling pathway in human cancers induced by infection with human papillomaviruses. Mol Cancer. 2015 Apr 17;14:87. [9] Pergialiotis V, Nikolaou C, Haidopoulos D, et al. PIK3CA Mutations and Their Impact on Survival Outcomes of Patients with Cervical Cancer: A Systematic Review. Acta Cytol. 2020;64(6):547-555. [10] Tan AC. Targeting the PI3K/Akt/mTOR pathway in non-small cell lung cancer (NSCLC). Thorac Cancer. 2020 Mar;11(3):511-518. [11] Wu SG, Chang YL, Yu CJ, et al. The Role of PIK3CA Mutations among Lung Adenocarcinoma Patients with Primary and Acquired Resistance to EGFR Tyrosine Kinase.