根据CSCO尿路上皮癌诊疗指南(2022),我们为大家详细的介绍目前转移性尿路上皮癌的标准治疗方案,以及最新的临床研究进展。

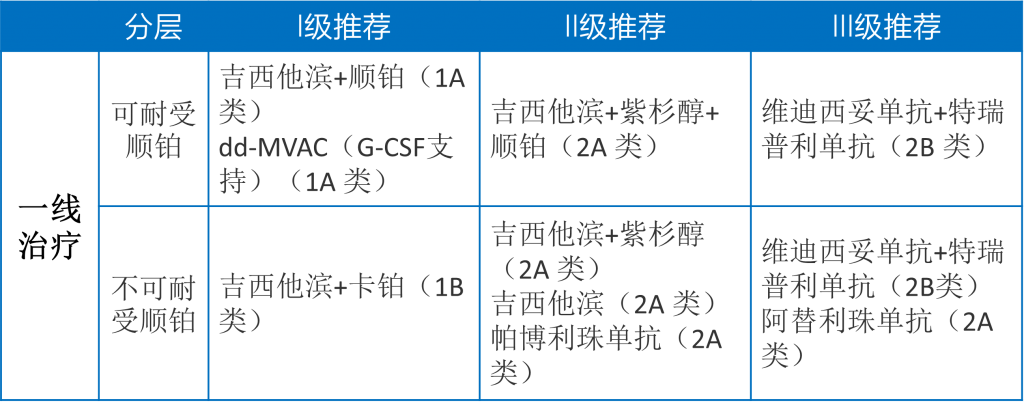
对于转移性尿路上皮癌,根据患者对铂类的耐受情况,可以分成可耐受顺铂和不可耐受的患者,具体推荐方案及推荐级别见表。此外,CSCO指南推荐一线化疗后客观有效或稳定的患者选择阿维鲁单抗(II级推荐)或帕博利珠单抗(III级推荐)进行维持治疗[1]。
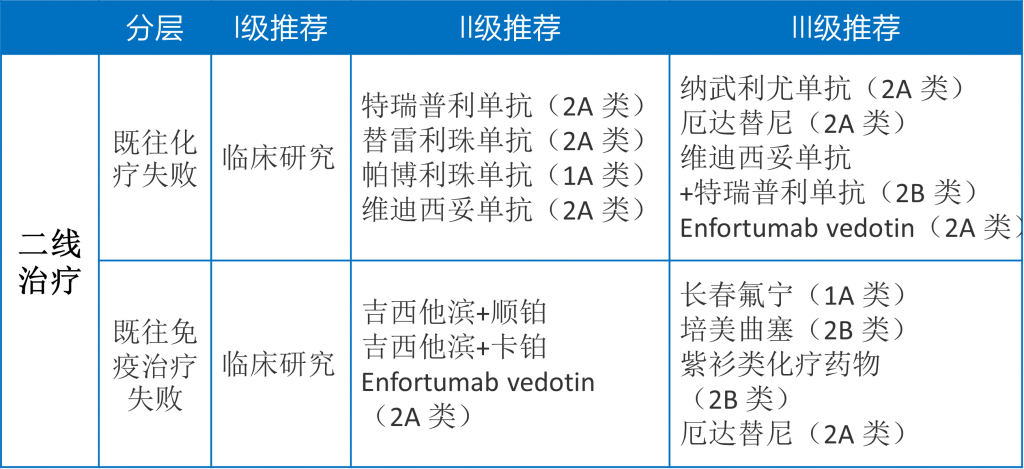
对于晚期膀胱癌的三线治疗,指南推荐PD-1/PD-L1 单抗免疫治疗用于既往未接受过免疫治疗的患者;对于免疫治疗失败同时携带FGFR2/3基因突变的患者,推荐厄达替尼治疗,具体见表[1]。

在转移性尿路上皮癌药物治疗方面,近年来多款药物或化合物有重要进展:
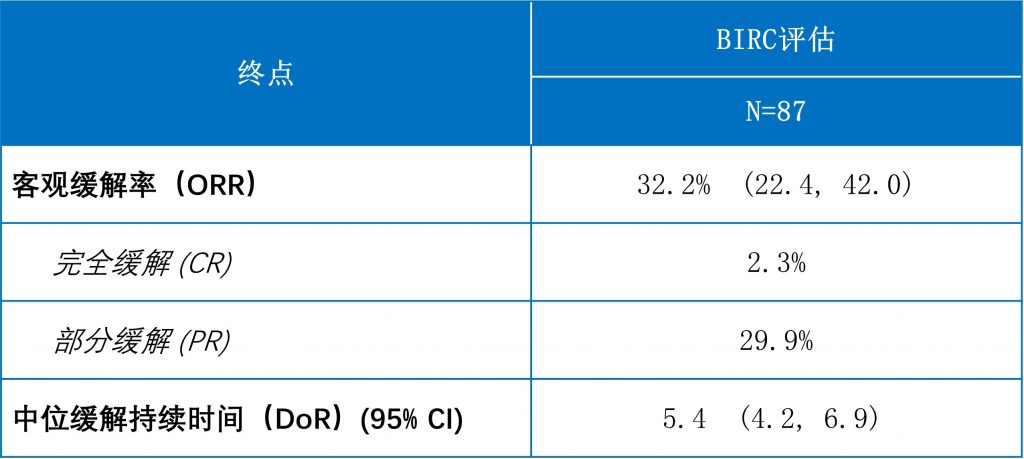
厄达替尼(erdafitinib)是一款靶向FGFR1/2/3/4的小分子抑制剂;基于BLC2001研究的早期结果,FDA于2019年4月加速批准erdafitinib用于治疗携带有FGFR3或FGFR2基因异常的、既往含铂治疗(包括12个月内新辅助或辅助含铂化疗)失败后疾病进展的局部晚期或转移性膀胱癌成人患者。BLC2001研究(NCT02365597)是一项多中心、II期单臂研究;入组患者为既往化疗失败的、携带FGFR3点突变(R248C、S249C、G370C、Y373C)或FGFR2/3基因融合(FGFR3-TACC3、FGFR3BAIAP2L1、FGFR2-BICC1、FGFR2-CASP7)的局部晚期或转移性尿路上皮癌患者。早期入组的87例疗效可评估的患者的疗效结果如表所示。该研究的最新数据显示,101例晚期FGFR基因突变的膀胱癌患者接受erdafitinib治疗后的客观缓解率为40%[2]。
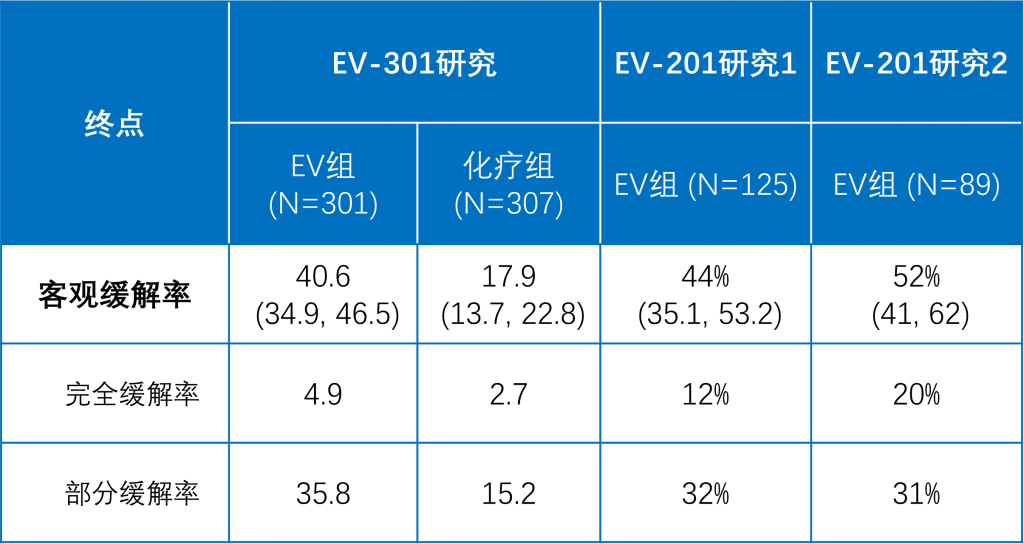
Enfortumab vedotin(EV)是由肿瘤表面分子nectin-4 的单克隆抗体与微管破坏剂MMAE组成的抗体偶联药物。基于EV-301和EV-201研究的结果,FDA已批准EV用于顺铂化疗失败或免疫治疗失败的转移性尿路上皮癌的治疗。EV-301研究是一项开放标签的III期随机对照研究,共纳入了608例既往PD-1/PD-L1抑制剂治疗和含铂化疗失败的晚期或转移性尿路上皮癌患者[3]。EV-201研究是一项多队列研究,其中队列1纳入了125例既往PD-1/PD-L1抑制剂治疗和含铂化疗失败的晚期或转移性尿路上皮癌患者[4],队列2纳入了89例既往PD-1/PD-L1抑制剂治疗失败但未接受过含铂化疗的局部晚期或转移性尿路上皮癌患者[5]。这三项研究的疗效结果见表。

目前在FGFR基因异常的膀胱癌或实体瘤患者中开展早期临床试验的FGFR抑制剂还有ICP-192(NCT04492293)、LOXO-435(NCT05614739)、TYRA-300(NCT05544552)等。在HER2异常的尿路上皮癌中,正在开展临床试验的有HER2-ADC药物trastuzumab-duocarmazine(NCT04602117)、pyrotinib (NCT05318339)。
此外,2022年ASCO上发布的两项随机对照II期研究表明携带DDR或HRR基因突变的患者可能从PARP抑制剂的单独治疗或组合治疗中获益。ATLANTIS研究结果表明rucaparib用于DNA损伤修复缺陷的mUC患者含铂化疗后的维持治疗时,显著延长了患者的PFS(HR=0.53,80% CI 0.30-0.92)[6];BAYOU研究则报道PD-L1抑制剂度伐利尤单抗(durvalumab)联合奥拉帕尼显著延长了HRR突变患者的PFS(HR=0.18,95% CI 0.06-0.47)[7]。
针对特定基因,作为新一代液态活检精准医疗国际领军企业——慧渡医疗,以外周血和尿液作为样本开发的靶向用药和MRD检测产品,具有灵敏度高和样本量要求低的优势。慧渡医疗系列基因检测产品获得国际最权威的美国FDA突破性医疗器械(BDD)认定(点击查看原文)、欧盟CE认证和英国UKCA认证(点击查看原文),这是国际权威监管机构对慧渡医疗技术、产品和其临床应用价值的认可。慧渡医疗新一代液态活检系列产品正被应用于全球排名前10的顶尖药企、美国哈佛大学等国际顶级学术机构开展的众多临床研究,推动国内、国际药企合作伙伴国际多中心临床试验、全球CDx伴随诊断开发和临床诊疗。
参考文献:
[1] CSCO尿路上皮癌诊疗指南(2022). [2] Siefker-Radtke AO, Necchi A, Park SH, et al. Efficacy and safety of erdafitinib in patients with locally advanced or metastatic urothelial carcinoma: long-term follow-up of a phase 2 study. Lancet Oncol. 2022 Feb;23(2):248-258. [3] Powles T, Rosenberg JE, Sonpavde GP, et al. Enfortumab Vedotin in Previously Treated Advanced Urothelial Carcinoma. N Engl J Med. 2021 Mar 25;384(12):1125-1135. [4] Rosenberg JE, O’Donnell PH, Balar AV, et al. Pivotal Trial of Enfortumab Vedotin in Urothelial Carcinoma After Platinum and Anti-Programmed Death 1/Programmed Death Ligand 1 Therapy. J Clin Oncol. 2019 Oct 10;37(29):2592-2600. [5] Yu EY, Petrylak DP, O’Donnell PH, et al. Enfortumab vedotin after PD-1 or PD-L1 inhibitors in cisplatin-ineligible patients with advanced urothelial carcinoma (EV‑201): a multicentre, single-arm, phase 2 trial.Lancet Oncol. 2021 Jun;22(6):e239. [6] JCO.2022.40.6_suppl.436. [7] JCO.2022.40.6_suppl.437.