
国际知名药企AstraZeneca为满足其抗肿瘤免疫药物的国际临床标准化,自主开发了用于鉴定血浆TMB(bTMB)检测能力的企业参考标准品(以下简称参考品),该方法发表于《Genes,Chromosomes & Cancer》杂志。AstraZeneca使用了慧渡医疗的PredicineATLAS™ 600基因液态活检作为评估其参考品性能的标准平台之一,充分体现了国际药企对慧渡医疗液态活检产品检测性能的信任。

TMB(Tumor mutational burden)是一类与肿瘤免疫治疗疗效相关的重要分子标志物,TMB检测的金标准是基于组织全外显子测序(WES)。WES的测序成本较高,而目前基于NGS panel设计的TMB检测产品在捕获区间、检测灵敏性和算法上的差异较大,致使TMB结果缺乏统一的评估标准,因此标准化TMB检测十分必要。而与组织相比,ctDNA具有创伤小、更容易进行多次连续采样和克服组织异质性的优点;此外,已有多个研究表明bTMB结果与组织TMB具有较高一致性,可以替代后者,因而bTMB在临床中的应用越来越广泛。
在本研究中,来自AstraZeneca的科研团队利用于恶性肿瘤患者的肿瘤细胞系模拟血浆游离DNA建立参考品,用于今后不同TMB分析平台的校准。首先,研究者利用不同方法(方法A和方法B),基于TMB值不同(7、9、20和26mut/Mb)的肺癌患者的肿瘤细胞系,建立了模拟ctDNA的参考品;然后,分别使用PredicineATLAS™和GuardantOMNI在第一阶段和第二阶段评估了方法A和B建立的模拟ctDNA参考品在不同肿瘤含量(2%和0.5%)的情况下用于TMB检测的性能表现。结果表明在2%肿瘤含量时,这两种方法建立的参考品中检出的突变及得到的TMB值都与组织WES的结果高度一致;但在0.5%的肿瘤含量时,自建参考品中检出的突变及得到的TMB值与WES的结果有差异,可能与肿瘤含量太低有关(图2)。
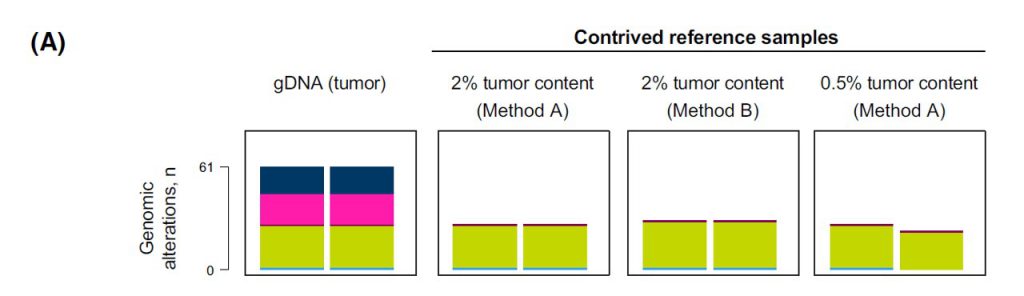
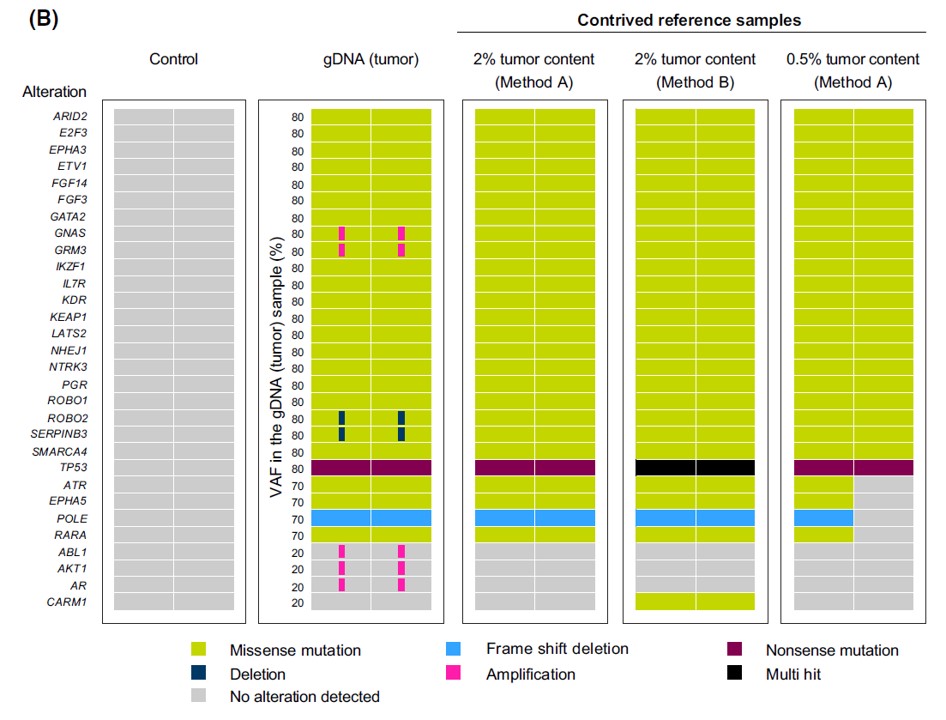
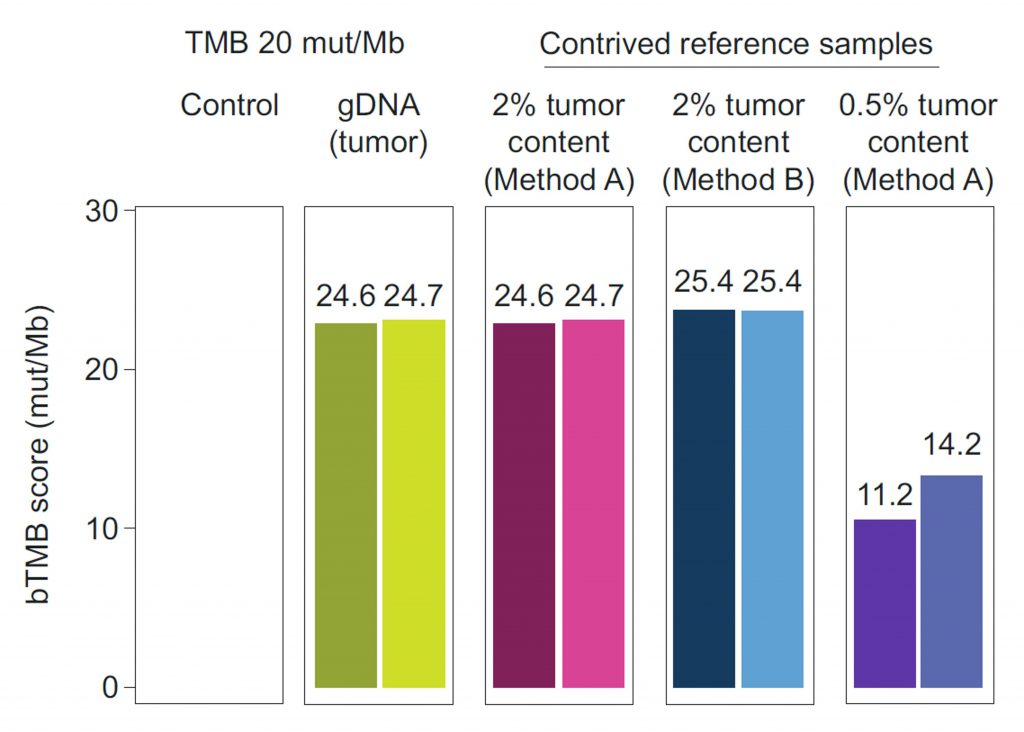
PredicineATLAS™ cfDNA 600产品是慧渡医疗自主开发的一款涵盖600个基因的NGS panel检测产品,捕获区间为2.4 Mb(其中编码区1.4 Mb)。2022年4月份,BMS北美团队对国际上认可度较高的5款大panel液态活检产品进行了性能测试,包括慧渡医疗的PredicineATLAS™ cfDNA 600基因检测产品(表中的assay B)。研究者们比较了这5款产品在检测实体瘤和髓系肿瘤中的常见突变时的性能表现,重点评估了这5款产品在不同DNA起始量(10ng、30ng或50ng cfDNA)和突变丰度(VAF,1%、0.5%、0.125%、0%)时检测SNVs和短插入/缺失时的能力。结果发现在DNA起始量只有10ng,突变丰度低至0.125%时,PredicineATLAS™ cfDNA 600的敏感性和特异性表现依然卓越。值得一提的是,慧渡医疗是唯一一款在所有测评条件下均未发生 “假阳性” 的参评产品(点击查看原文)。
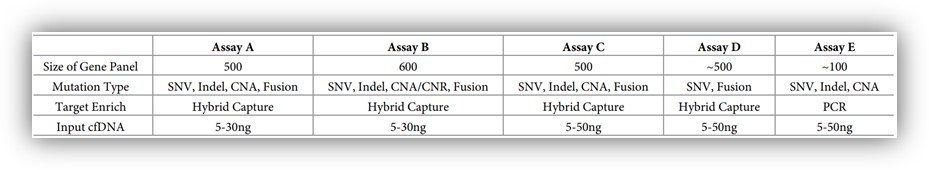
*注:Assay B是慧渡医疗600基因的PredicineATLAS™。
目前慧渡医疗与全球前十名的国际药企进行临床合作研究,多篇文章发表在THE LANCET Gastroenterology & Hepatology等影响因子达45分的国际顶级学术期刊。慧渡医疗新一代液态活检技术灵敏度高、样本要求量低。PredicineCARE™获得国际最权威的美国FDA突破性医疗器械认定(点击查看原文)、欧盟CE认证和英国UKCA认证(点击查看原文),这是国际权威监管机构对慧渡医疗技术、产品和其临床应用价值的认可和背书。
慧渡医疗坚持 “起点就是业界顶点” 的从业标准,打造液态活检国际精品。从欧美药企出发,通过在中美同步运营的CAP和CLIA实验室网络,提供中美一致的检测产品和服务,为药企临床试验和患者提供全球一致的检测服务和一站式生物标志物分析,助力药企全球新药临床试验和CDx开发。
慧渡医疗将一如既往联手全球跨国药企、世界顶尖医疗机构和各界合作伙伴们,为全球肿瘤患者和药企提供最优质的产品和服务,早日实现公司的愿景 —— “把最好的医院送到每个村庄,把最好的医生送到每个家庭” 。
